Съдържание
- 1 Отглеждане на органи от стволови клетки
- 1.1 Какво представляват стволовите клетки?
- 1.2 Какви органи и тъкани са успели да отглеждат учените с помощта на стволови клетки?
- 1.3 През 2005 г. американски учени за първи път отглеждат пълноценни мозъчни клетки.
- 1.4 През 2005 г. учените успяха да възпроизведат невронна стволова клетка
- 1.5 През 2006 г. швейцарски учени са отгледали сърдечни клапи на човешкото тяло от стволови клетки
- 1.6 През 2006 г. британски учени отглеждат чернодробна тъкан от стволови клетки
- 1.7 През 2006 г. сложен човешки орган - пикочния мехур - беше отгледан за първи път в САЩ.
- 1.8 Американски учени успяха да отглеждат пълноценен пикочен мехур в лаборатория. Клетките на самите пациенти, нуждаещи се от трансплантация, бяха използвани като материал.
- 1.9 През 2007 г. стволовите клетки помогнаха на британските учени да създадат част от човешкото сърце
- 1.10 През 2007 г. японски учени отглеждат роговицата на окото от стволови клетки
- 1.11 През 2007 г. японски учени израснаха зъб от стволови клетки
- 1.12 През 2008 г. американски учени успяха да отгледат ново сърце върху скелет от старото
- 2 Отглеждане на органи от стволови клетки
- 3 Нов начин за отглеждане на органи за трансплантация (видео)
- 4 Състояние на техниката
- 4.1 Ембриоиди
- 4.2 Органоиди на сърдечно -съдовата тъкан
- 4.3 Чернодробни органели
- 4.4 Органоиди на слюнчените и слъзните жлези
- 4.5 Бъбречни органели
- 4.6 Органели на панкреаса
- 4.7 Тимусни органели
- 4.8 Органели на белодробната тъкан
- 4.9 Органели на ретината
- 4.10 Органели на сензорния епител на вътрешното ухо
- 4.11 Органели на простатата
- 4.12 Церебрални органели
- 4.13 Епителни ентероиди, колоноиди и холангиоиди
- 4.14 Сфероиди на космените фоликули
- 4.15 Биоинженерен мускул
- 4.16 Хрущялна и мускулна тъкан за реконструкционни операции
- 4.17 Преодоляване на имунното отхвърляне на органите
- 4.18 3D биопечат
- 5 Ролята на тъканната самоорганизация
- 6 Роля на извънклетъчния матрикс
- 7 Вижте също
- 8 Бележки (редактиране)
- 9 Литература
Отглеждане на органи от стволови клетки
Преди да преминем към директната история за отглеждането на органи, бих искал да ви посветя какво представляват стволовите клетки.
Какво представляват стволовите клетки?

Стволови клетки - прародителите на всички видове клетки в тялото, без изключение. Те са способни на самообновяване и най-важното в процеса на разделяне те образуват специализирани клетки от различни тъкани. Стволовите клетки се обновяват и заменят клетките, загубени в резултат на увреждане във всички органи и тъкани. Те са предназначени да възстановят човешкото тяло от момента на раждането му.
С възрастта броят на стволовите клетки в тялото намалява драстично. При новородено 1 стволова клетка се открива на 10 хиляди, на възраст 20-25 години - 1 на 100 хиляди, на 30 - 1 на 300 хиляди. До 50 -годишна възраст в тялото остава само 1 стволова клетка на 500 хиляди. Изчерпването на стволовите клетки поради стареене или сериозни заболявания лишава организма от способността да се самолекува. Поради това жизнената дейност на определени органи става по -малко ефективна.
Какви органи и тъкани са успели да отглеждат учените с помощта на стволови клетки?
Цитирам само най -известните примери за научни постижения.
през 2004 г. японски учени са първите в света, които отглеждат структурно завършени капилярни кръвоносни съдове от стволови клетки

Японските учени са първите в света, които отглеждат структурно завършени капилярни кръвоносни съдове от човешки ембрионални стволови клетки. Това съобщи на 26 март 2004 г. японският вестник Yomiuri.
Според публикацията група изследователи от Медицинския факултет на Киото, ръководена от професор Казува Накао, са използвали капилярни клетки, генерирани от стволови клетки, внесени от Австралия през 2002 г. Досега изследователите са успели да регенерират само нервни клетки и мускулна тъкан, което не е достатъчно, за да „произведе“ цял орган. Информация от сайта
През 2005 г. американски учени за първи път отглеждат пълноценни мозъчни клетки.
Учени от Университета на Флорида (САЩ) са първите в света, които отглеждат напълно оформени и присадени мозъчни клетки. Според ръководителя на проекта Бьорн Шефлер, клетките са отгледани чрез „копиране“ на регенерацията на мозъчните клетки. Сега учените се надяват да отглеждат клетки за трансплантация, което би могло да помогне за лечение на болестта на Алцхаймер и Паркинсон. Шефлър отбеляза, че по -ранните учени са успели да отглеждат неврони от стволови клетки, но именно във Флоридския университет те са успели да получат пълни клетки и да проучат процес на растежа им от началото до края. Информация от сайта Gazeta.ru въз основа на материалите на Independent.
През 2005 г. учените успяха да възпроизведат невронна стволова клетка
нервна стволова клетка
Италианско-британска група учени от университетите в Единбург и Милано се научи как да създава различни видове клетки на нервната система in vitro на базата на неспециализирани ембрионални стволови клетки.
Учените са приложили вече разработени методи за контрол на ембрионалните стволови клетки към по -специализираните невронни стволови клетки, които са получили. Резултатите, които са постигнати в миши клетки, са репликирани в човешки стволови клетки. В интервю за Би Би Си Стивън Полард от Университета в Единбург обясни, че развитието на колегите му ще помогне за пресъздаването на болестта на Паркинсон или Алцхаймер ин витро. Това ще позволи по-добро разбиране на механизма на тяхното възникване и развитие, както и ще предостави на фармаколозите мини полигон за търсене на подходящи лечения. Съответните преговори с фармацевтичните компании вече са в ход.
През 2006 г. швейцарски учени са отгледали сърдечни клапи на човешкото тяло от стволови клетки
През есента на 2006 г. д -р Саймън Херстрап и колегите му от университета в Цюрих за първи път отглеждат сърдечни клапи на човека, използвайки стволови клетки, взети от околоплодната течност.
Това постижение би могло да направи възможно отглеждането на сърдечни клапи специално за нероденото дете, ако се открият сърдечни дефекти в утробата. И скоро след раждането на бебето може да се трансплантират нови клапи.
След култивирането на пикочния мехур и кръвоносните съдове от човешки клетки в лаборатория, това е следващата стъпка към създаването на „собствени“ органи за конкретен пациент, способни да премахнат необходимостта от донорски органи или изкуствени механизми.
През 2006 г. британски учени отглеждат чернодробна тъкан от стволови клетки
През есента на 2006 г. британски учени от университета в Нюкасъл обявиха, че те са първите в света, които отглеждат изкуствен черен дроб в лабораторни условия от стволови клетки, взети от кръвта от пъпната връв. Техниката, използвана за създаване на 2 см мини-черен дроб, ще бъде допълнително развита, за да се създаде нормално функциониращ черен дроб със стандартен размер.
През 2006 г. сложен човешки орган - пикочния мехур - беше отгледан за първи път в САЩ.

Американски учени успяха да отглеждат пълноценен пикочен мехур в лаборатория. Клетките на самите пациенти, нуждаещи се от трансплантация, бяха използвани като материал.
„С биопсия можете да вземете парче тъкан и след два месеца количеството му ще се умножи няколко пъти“, обяснява директорът на Института по регенеративна медицина Антъни Атала. „Слагаме изходния материал и специалните вещества в специална форма, оставяме ги в специален лабораторен инкубатор и след няколко седмици получаваме готов орган, който вече може да бъде трансплантиран.“ Първата трансплантация е извършена в края на 90 -те години. Операция по трансплантация на пикочен мехур е извършена на седем пациенти. Резултатите отговарят на очакванията на учените и сега експертите разработват методи за създаване на още 20 органа - сред тях сърцето, черния дроб, кръвоносните съдове и панкреаса.
През 2007 г. стволовите клетки помогнаха на британските учени да създадат част от човешкото сърце
През пролетта на 2007 г. група британски учени, състояща се от физици, биолози, инженери, фармаколози, цитолози и опитни клиницисти, ръководена от професор по кардиохирургия Магди Якуб, за първи път в историята успяха да пресъздадат един от типовете човешка сърдечна тъкан, използваща стволови клетки от костен мозък. Тази тъкан действа като сърдечни клапи. Ако допълнителните тестове са успешни, разработената техника може да се използва за отглеждане на пълноценно сърце от стволови клетки за трансплантация на пациенти.
През 2007 г. японски учени отглеждат роговицата на окото от стволови клетки
През пролетта на 2007 г. на симпозиум по репродуктивна медицина в град Йокохама бяха обявени резултатите от уникален експеримент от специалисти от Токийския университет. Изследователите са използвали стволови клетки, взети от ръба на роговицата. Такива клетки са в състояние да се развият в различни тъкани, изпълнявайки възстановителни функции в организма. Изолираната клетка се поставя в хранителна среда. Седмица по -късно се развива в група клетки, а през четвъртата седмица се трансформира в роговица с диаметър 2 см. По същия начин се получава тънък защитен слой (конюнктива), покриващ роговицата от навън.
Учените подчертават, че за първи път от една клетка е отгледана пълноценна човешка тъкан. Трансплантацията на органи, получена по нов метод, елиминира риска от предаване на инфекции. Японските учени възнамеряват да започнат клинични изпитвания веднага след като се убедят в безопасността на новата технология.
През 2007 г. японски учени израснаха зъб от стволови клетки
Японски учени са успели да отгледат зъб от една клетка. Отглежда се в лаборатория и се трансплантира в мишки. Клетъчният материал се инжектира в колагеновото скеле. След култивирането се оказа, че зъбът е придобил зряла форма, която се състои от цели части като дентин, пулпа, съдове, пародонтални тъкани и емайл. Според изследователите зъбът е идентичен с естествения. След трансплантацията на лабораторен миши зъб, той е присаден и функционира напълно нормално. Техниката ще позволи да се отглеждат цели органи от една или две клетки, казват изследователите.
През 2008 г. американски учени успяха да отгледат ново сърце върху скелет от старото
Дорис Тейлър и нейните колеги от университета в Минесота създадоха живо сърце на плъх, използвайки необичайна техника. Учените взеха сърце на възрастен плъх и го поставиха в специален разтвор, който премахна всички клетки на тъканта на сърдечния мускул от сърцето, оставяйки останалите тъкани непокътнати. Това пречистено скеле беше посято с клетки на сърдечния мускул от новородено плъх и поставено в среда, която имитира условията в тялото.
Само след четири дни клетките се умножиха толкова много, че новата тъкан започна да се свива и след осем дни реконструираното сърце вече беше в състояние да изпомпва кръв, макар и само на ниво от 2 % мощност (броене от здраво сърце на възрастен). Така учените са получили работещ орган от клетките на второ животно. По този начин в бъдеще би било възможно да се обработват сърца, взети за трансплантация, за да се изключи отхвърлянето на органи. „Можете да правите всеки орган като този: бъбрек, черен дроб, бял дроб, панкреас“, казва Тейлър. Донорското скеле, което определя формата и структурата на органа, ще бъде изпълнено със специализирани клетки, направени от стволови клетки, които са естествени за пациента.
Любопитно е, че в случай на сърце, като основа, можете да опитате да вземете сърце на прасе, анатомично близко до човешко. Чрез премахване само на мускулна тъкан, други тъкани на такъв орган вече могат да бъдат допълнени с култивирани човешки сърдечни мускулни клетки, като се получи хибриден орган, който на теория трябва да се вкорени добре. И новите клетки веднага ще бъдат добре снабдени с кислород - благодарение на старите съдове и капиляри, останали от сърцето на донора.
Килере 28.01.2009

Медицински учен на работа
В продължение на много години учените по целия свят работят за създаването на работещи тъкани и органи от клетки. Най -често срещаната практика е отглеждането на нови тъкани от стволови клетки. Тази технология е тествана в продължение на много години и е постоянно успешна.Но все още не е възможно да се осигури напълно необходимия брой органи, тъй като е възможно да се отгледа орган за конкретен пациент само от неговите стволови клетки.
Учени от Великобритания са успели в това, което никой не е успял да направи досега - да препрограмира клетките и да отгледа от тях работещ орган. Това ще позволи в обозримо бъдеще да се предоставят органи за трансплантация на всички, които ще се нуждаят от това.
Отглеждане на органи от стволови клетки
Отглеждането на органи от стволови клетки е познато на лекарите от дълго време. Стволовите клетки са предшественици на всички клетки в тялото. Те могат да заменят всички повредени клетки и са предназначени за възстановяване на тялото. Максималният брой на тези клетки се среща при деца след раждането и броят им намалява с възрастта. Следователно постепенно способността на организма да се лекува намалява.
 Изработването на органи от клетки е сложен и скъп процес
Изработването на органи от клетки е сложен и скъп процес
В света вече са създадени много напълно функциониращи органи от стволови клетки, например през 2004 г. в Япония от тях са създадени капиляри и кръвоносни съдове. А през 2005 г. американски учени успяха да създадат мозъчни клетки. През 2006 г. в Швейцария са създадени човешки сърдечни клапи от стволови клетки. През същата 2006 г. чернодробната тъкан е създадена във Великобритания. Досега учените са се занимавали с почти всички тъкани на тялото, дори със пораснали зъби.
В САЩ беше направен много любопитен експеримент - там беше отгледано ново сърце върху рамка от старото. Сърцето на донора беше изчистено от мускули и бяха изградени нови мускули от стволови клетки. Това напълно изключва възможността за отхвърляне на донорския орган, тъй като той става „негов“. Между другото, има предположения, че като рамка ще бъде възможно да се използва свинско сърце, което анатомично много прилича на човешко.
Нов начин за отглеждане на органи за трансплантация (видео)
Основният недостатък на съществуващия метод за отглеждане на органи е необходимостта от тяхното производство на собствените стволови клетки на пациента. Не всеки пациент може да приема стволови клетки и още повече, не всеки има готови замразени клетки. Но наскоро иИзследователи от университета в Единбург са успели да препрограмират клетките на тялото, така че да могат да отглеждат необходимите органи от тях. Според прогнозите широкото използване на тази технология ще стане възможно след около 10 години.
Към днешна дата учените вече са успели да създадат напълно функционираща тимусна жлеза, която регулира имунната система и се намира до сърцето. Този орган е направен от клетки от просо съединителна тъкан, която е получена от ембрион на мишка. Клетките на съединителната тъкан са трансплантирани в друга клетъчна култура благодарение на специален "генетичен превключвател" в ДНК.
Досега опитите с отглеждане на органи по този начин не дават осезаеми резултати. Това е първият успешен експеримент, който показа, че е възможно да се отгледа желаният орган дори без използването на стволови клетки, и с помощта на всякакви други клетки на тялото, например клетки от съединителна тъкан.
Здравейте! Аз съм Алиса. Какво мога да кажа за себе си? Привърженик на здравословния начин на живот.
Растящи органи - обещаваща биоинженерна технология, чиято цел е да създаде различни пълноценни жизнеспособни биологични органи за хората. Понастоящем технологията не се използва при хора, тъй като всички опити за трансплантация на такива органи са неуспешни, но има активни разработки и експерименти в тази област. Използвайки триизмерни клетъчни култури, учените са се научили да отглеждат "зачатъци" на органи, наречени органели (Английски... органоид, да не се бърка с органели).Такива органели се използват от учените за изучаване и моделиране на органогенезата, моделиране на тумори и различни заболявания, които могат да засегнат определени органи, тестване и скрининг на различни лекарства и токсични вещества върху органоидите, както и за експерименти по подмяна на органи или лечение на увредени органи с трансплантации.
Състояние на техниката
Идеята за изкуствено растящи човешки органи се появява в средата на 20 -ти век, от момента, в който донорските органи започват да се трансплантират при хора. Дори и с възможността за трансплантация на повечето органи на пациенти, въпросът за донорството в момента е много остър. Голям брой пациенти умират, без да чакат органа си. На теория отглеждането на изкуствени органи може да спаси милиони човешки животи. Някои напредъци в тази посока вече са постигнати с помощта на методи за регенеративна медицина.
Ембриоиди
Ембриоидите или ембрионалните тела са триизмерни агрегати от клетки, където са представени клетки от трите зародишни слоя, които са необходими за образуването на органи и тъкани на тялото. При лабораторни условия те могат да бъдат получени чрез различни методи на отглеждане от недиференцирани iPSC. Формирането на ембрионално тяло е често срещан метод, използван за диференциране на iPSCs в различни клетъчни линии.
Органоиди на сърдечно -съдовата тъкан
Чрез култивиране на ембриоиди върху конюгирани с колаген хидрогели с твърдост, подобна на тази на сърдечната мускулна тъкан, Shkumatov et al. успя да получи сърдечно -съдови органели, способни на свиване. По този начин те показаха, че твърдостта на извънклетъчния матрикс може да играе важна роля в клетъчната диференциация. Необходимостта от създаване на механични напрежения, които са удобни за култивираните клетки чрез регулиране на твърдостта на субстратния материал за отглеждане, беше отбелязана в редица други работи. Новите технологии направиха възможно синхронизирането на контракциите на клетките на сърдечния органоид. Правилно подбраният темп на електрическо стимулиране, принуждавайки нарастващата мускулна тъкан да се свива, позволява не само да се съкрати времето за култивиране, но и да се копира по -качествено зрялата здрава сърдечна тъкан в редица параметри.
Чернодробни органели
Изследователи от Япония са направили важна крачка към отглеждане на органи в лабораторията. Те успяха да създадат прост, но напълно функционален човешки черен дроб. Изследователите са получили чернодробни клетки от iPSCs и са ги култивирали заедно с ендотелни клетки (предшественици на кръвоносните съдове) и мезенхимни клетки, които действат като "лепило", което обединява различни клетки. Оказа се, че при определено съотношение на тези клетки, тяхната съвместна култура проявява способността да се самоорганизира и образува триизмерни сферични структури, които представляват зачатъка на черния дроб. Когато тези чернодробни пъпки бяха трансплантирани в мишки, беше установено, че за около 48 часа те образуват връзки с близките кръвоносни съдове и са в състояние да изпълняват функции, характерни за черния дроб. Според някои учени такива зачатъци на черния дроб, ако бъдат намалени по размер и след това въведени в кръвния поток на увредения черен дроб, биха могли да помогнат за нормализиране на неговата функция. За съжаление, все още няма гаранция, че чернодробните клетки, получени от iPSCs, няма да предизвикат образуването на тумори. Необходимо е внимателно усъвършенстване на тези методи. На базата на чернодробни органели е създадено устройство - био -изкуствен черен дроб с чернодробни органели за временна поддръжка на живота на пациентите.
Takebe et al. създаде възпроизводим метод за мащабно отглеждане на васкуларизирани човешки чернодробни органели изцяло от индуцирани плурипотентни стволови клетки (iPSCs) и демонстрира тяхната функционалност за използване като трансплантация за лечение на хора.
Органоиди на слюнчените и слъзните жлези
Екип от изследователи от Токийския университет за наука и корпорация Organ Technologies Inc. ръководен от професор Такаши Цуджи (Такаши цуджи) демонстрира функционалната регенерация на субмандибуларните слюнчени жлези от биоинженерни ембриони на слюнчените жлези след тяхната ортотопична (с отстраняване на дефектната жлеза) трансплантация, с цел възстановителна терапия чрез подмяна на органа при мишки, при който е моделиран дефектът на слюнчените жлези . Създаденият биоинженериран ембрион се е развил в зряла жлеза чрез образуването на увиформени процеси с мускулен епител и инервация. Той произвежда и отделя слюнка в отговор на стимулация на вкуса с цитрат, възстановява процеса на поглъщане на храна и предпазва устната кухина от бактериална инфекция. Същата група успешно извърши ортотопична трансплантация на биоинженерни ембриони на слъзните жлези в мишки с модел, симулиращ увреждане на епитела на роговицата, причинено от дисфункция на слъзната жлеза. In vivo, биоинженерните ембриони пораждат слъзни жлези, способни да изпълняват физиологични функции, включително производство на сълзи в отговор на нервна стимулация и защита на очната повърхност.
Бъбречни органели
Разработени са технологии за отглеждане на бъбречни органели от плурипотентни клетки, които могат да се използват за симулиране на бъбречни заболявания и скрининг на лекарства за тяхното лечение, а в бъдеще и за имплантиране на миниатюрни бъбреци при пациенти, създадени от собствени iPSCs. Разработена е стратегия за трансплантация на такъв органоид, която му позволява да източва отделената от него урина в пикочния мехур.
Органели на панкреаса
Изследователи от Датския център за стволови клетки са разработили триизмерна (3-D) гел култура Матригел със специално подбран състав на средата, който може да се използва за отглеждане на миниатюрни "семена" на панкреаса. В дългосрочен план такива „рамки“ могат да бъдат полезни за борбата с диабета като „резервни части“.
Тимусни органели
Тимусът играе важна роля в генерирането на нови Т клетки. Тази жлеза е много активна в ранна възраст, но умира след достигане на зряла възраст в процес, известен като тимусна инволюция, което води до намаляване на имунитета при възрастните хора. Инжектирането на тимусни органели в тялото на възрастни хора би могло да им помогне да се преборят с редица старчески заболявания. Експериментите за отглеждане на тимусни органоиди и тяхната трансплантация в атимични мишки дават надежда в това отношение. Оказа се, че тимусните органели не само могат да се вкоренят, но и могат ефективно да допринесат за възстановяването на функцията на тимуса при неговите реципиенти. В бъдеще тимусните органоиди ще направят възможно производството на модифицирани Т-клетки в биореактори за целенасочена борба с рака.
Органели на белодробната тъкан
Чрез въздействие върху сигналните пътища на човешки iPSCs, беше възможно да се получат органели на човешките бели дробове, състоящи се от епителни и мезенхимни белодробни отделения, със структурни характеристики, характерни за белодробните тъкани. Модификация на този метод дава възможност да се отглеждат органели от белодробна тъкан в биореактор и да се използват за изследване на белодробни заболявания.
Органели на ретината
Развити 3-D органели на очната ябълка и ретината с фоторецепторни клетки: пръчки и конуси. Това ще позволи в бъдеще да се разработят методи за лечение на очни заболявания като дегенерация на ретината.
Органели на сензорния епител на вътрешното ухо
Подобна технология е използвана за разработване на методи за получаване на органели в сензорния епител на вътрешното ухо, което в бъдеще ще помогне за борба с глухотата.
Органели на простатата
Органоидите на простатата са получени чрез насочена диференциация на ESCs. Отбелязва се, че времето на излагане на факторите WNT10B / Fgf10, които играят ключова роля при формирането на простатата, както и по време на вътрематочното развитие, е от решаващо значение за образуването на епителни клетки на простатата.
Церебрални органели
За целите на моделиране и изследване инвитро на човешкия мозък и неговите заболявания е създадена триизмерна култура от органели от мозъчни клетки, получени от плурипотентни стволови клетки. Церебрални органели (Английски... Церебрален органоид) може да се използва за изследване на нерулирането и други процеси на неврогенезата, като прости модели на сложна мозъчна тъкан за изследване на ефектите на токсините и лекарствата върху мозъчната тъкан чрез техния безопасен и рентабилен първоначален скрининг, както и за получаване на проби за ксенотрансплантация.
Епителни ентероиди, колоноиди и холангиоиди
При моделирането на епителни органи проблемът е разнообразието от източници на епителни тъкани, изключителната чувствителност на пролиферативната активност на епителните клетки към външни промени, както и особеностите, свързани с епитело-мезенхимния преход, които са характерни изключително за епителните тъкани . Тъй като формата на такива тъкани е предимно стена, възстановяването й е свързано с многослойна организация и функционалност (перисталтика, нервна регулация). Тези характеристики на морфологията на тъканите обобщават биологичните проблеми, възникващи при търсенето на нови ефективни методи за възстановителна и регенеративна хирургия на стените на кухи епителни органи (хранопровод, стомах, черва), както и тръбни структури (жлъчен канал, уретер). Органелите, получени от епителни клетки на тънките и дебелите черва, ще помогнат за изследването на човешкото черво. Те могат да се използват за изследване на чревни стволови клетки и механизми на нарушаване на физиологичните функции на стомашно -чревния тракт, както и за създаване на туморни органели за изследване на рак и скрининг на лекарства.
Сфероиди на космените фоликули
Техниката на отглеждане на клетки под формата на сфероиди във висяща капка е използвана за култивиране на клетки от папиларния слой от човешки космени фоликули. Доказано е, че когато тези клетки се отглеждат под формата на сфероиди, когато клетките растат в по-естествена триизмерна среда и взаимодействат помежду си, те са в състояние да индуцират отново образуването на космените фоликули в човешката кожа.
Биоинженерен мускул
Създадена е така наречената "мускулна" тъкан, която реагира на сигнали от нерва благодарение на нервно-мускулната връзка, израснала от мускулни клетки и невронни клетки. Тази тъкан потенциално може да се използва за фармакокинетични анализи и за създаване на мускулен двигател за биороботи и протези. Освен това, отглеждани инвитро Биоинженерният мускул се оказа способен за развитие, регенерация и успя да се вкорени след трансплантацията му в животно. Разработена е технология за получаване на мускули от iPSCs, която може да се умножава за неопределено време чрез култивиране, което ще направи възможно отглеждането на мускулна тъкан в големи количества
Хрущялна и мускулна тъкан за реконструкционни операции
От малък брой клетки в носната преграда на пациентите е било възможно да се отгледа хрущялна тъкан, която се използва за реконструкция на носа след отстраняване на тумора. След повече от една година всички пациенти бяха доволни от естетическите и функционалните резултати от операцията и не бяха регистрирани отрицателни ефекти.
Тъканните импланти, отглеждани в лаборатория от собствени мускулни и епителни клетки на жени, които се нуждаят от операция за реконструкция на влагалището, не само успешно се вкореняват и функционират след пластична хирургия.
Създаден е субстрат и специален инкубатор за отглеждане на хранопровода на човека от пациентски клетки. В дългосрочен план това развитие ще спаси живота на новородените, родени без значителна част от хранопровода.
Преодоляване на имунното отхвърляне на органите
Важна пречка при трансплантацията на тъкани и органи е тяхното отхвърляне. Дори ако алотрансплантатът е успешен, пациентът с трансплантация на органи обикновено трябва да приема лекарства против отхвърляне до края на живота си.За да се направи присадката „невидима“ за човешката имунна система, е създадена култура от човешки ембрионални стволови клетки, които синтезират две молекули, които потискат активността на Т клетките, а именно CTLA4-Ig (Цитотоксичен антиген-4-имуноглобулин, свързан с Т лимфоцити) и PD-L1 (Програмиран лиганд на смърт 1), както преди, така и след диференциацията. Характеристика на тези клетки е, че образуваните от тях алогенни (от друго лице) тъкани не предизвикват имунна реакция и отхвърляне след трансплантация. Това означава, че трансплантацията на органи и тъкани, отгледани от тези „универсални“ клетки, може да бъде възможно да се извърши без да е необходимо да се проверява за съвместимост.
3D биопечат
3D Bioprinting Solutions е първият в света, който създава функционираща щитовидна жлеза на мишка, използвайки 3D биопечат. Руският биопринтер FABION се използва за отпечатване на щитовидната жлеза от клетки, взети от мишки. Отпечатаните органи са трансплантирани в мишки, чиято щитовидна жлеза е унищожена с радиоактивен йод. Резултатите от работата бяха представени от авторите на различни научни конференции и публикувани в рецензирани списания за специалисти.
Ролята на тъканната самоорганизация
Вижте също Синтетична морфогенеза
Учените все още не могат да обяснят как клетките се самоорганизират в сложни тъкани. Подредените структури възникват от клетки без външни сили или влияние. По време на развитието си клетките влияят помежду си на поведението и вземат решения въз основа на „разговор“ със съседите. Според японски учен Сасаи„Такива явления на самоорганизация могат да се видят само в групи от приблизително 1000 до 100 000 клетки. На това ниво клетките могат да бъдат директно демократични; те не се нуждаят от специален управител или президент, който да ги организира. " Клетките са "сортирани": един и същи тип се слепват, докато различните типове остават разединени. По-късно възникват центрове на организация, които ръководят морфогенезата чрез изолиране на растежни фактори (морфогени), използвайки градиенти, чиито концентрации създават така наречените биополета. Пример за практическото приложение на градиентите на концентрация е индуцираният растеж на аксони по градиентите на концентрация на специфични цитокини.
Процесът на самоорганизация на клетъчната култура в органели може да се контролира чрез избор на необходимите компоненти на 3D средата. Важно е да се отбележи, че едни и същи органели могат да бъдат получени с помощта на различни среди. Важно е само да се даде правилния "стартов" сигнал, а механизмът за самоорганизация ще свърши останалото.
Роля на извънклетъчния матрикс
За нормално функциониране и обновяване на тъканните клетки в тялото е необходим междуклетъчен матрикс, който създава, поддържа и регулира условията за тяхното съществуване в ниша. Извънклетъчната матрица е многофункционална система, която активно участва в различни процеси, свързани с развитието на тялото, като често играе ролята на „намек“, който ръководи диференциацията на клетките в една или друга посока. Компонентите на матрицата могат да бъдат разделени на две условни групи: структурни протеини, като фибриларни протеини и гликозаминогликани, и регулаторни протеини, включително всички видове растежни фактори, матрични клетъчни протеини (протеини от семейство CCN, IGFBP, декорин и бигликан) , ензими (металопротеинази) и рецептори (интегрини). Все още не е възможно да се пресъздаде такава сложна органна система и архитектура чрез изкуствени средства, например с помощта на 3D биопечат. Учените обаче са разработили технологии за получаване на извънклетъчен матрикс от алотрансплантати на донорски органи чрез измиването им с разтвори на детергенти, по време на които донорските клетки се отстраняват и остава само безклетъчната матрица, която все още запазва архитектурата (включително мрежата от кръвоносни и лимфни съдове и матрикса на нервната тъкан), а също и повечето регулаторни протеини. След това тази матрица се засява с клетките на реципиента и се поставя в биореактор и могат да се използват различни технологии за колонизация на матрицата и нейното култивиране, включително комбинирани такива: например 3D биопечатване, статично и динамично култивиране.В резултат на това е възможно да се отгледа автотрансплантат, който се състои от клетките на реципиента и на теория не бива да се отхвърля от имунната му система. Тази технология позволява безклетъчната матрица, получена от сърцето на донора, да бъде населена с кардиомиоцити, получени от iPSC на реципиента и да отгледа функциониращ сърдечен мускул от тях в инкубатор, който им доставя хранителен разтвор, а също така възпроизвежда някои параметри на околната среда на живия организъм.
Разработена е протеза на трахеята, която е 95% съставена от тъканите на пациента, което избягва отхвърлянето на органи. Скелетът на протезата е кост, израснала от периостална тъкан. Вътрешната повърхност на органа е създадена от стволови клетки и собствена лигавица на пациента. Биореакторът, в който новата трахея узрява в продължение на шест месеца, е тъканта на гръдната стена на пациента. В резултат на инкубацията в протезата се формира собствена съдова система.
Вижте също
- Автотрансплантация
- Растящи зъби
- Отглеждане на тимус от iPSCs
- Децелуларизация
- Отглеждане на човешки органи и тъкани при животни
- Синтетична морфогенеза
- 3D биопечат
Бележки (редактиране)
- ↑ Водещите хирурзи предупреждават срещу медийния шум за регенерацията на трахеята. Посетен на 2 юли 2017 г.
- ↑ Cantrell MA, Kuo CJ. (2015). Моделиране на органоиди за прецизна медицина за рак. Genome Med.; 7 (1): 32. DOI: 10.1186 / s13073-015-0158-y.PMID 25825593
- ↑ Lancaster MA, Knoblich JA. (2014). Генериране на мозъчни органоиди от човешки плюрипотентни стволови клетки. Nat Protoc.; 9 (10): 2329-40. DOI: 10.1038 / nprot.2014.158. PMID
- ↑ Habka D, Mann D, Landes R, Soto-Gutierrez A (2015) Бъдеща икономика на чернодробната трансплантация: 20-годишна прогноза за моделиране на разходите и перспективата за автоинженерни автоложни чернодробни присадки. PLoS ONE 10 (7): e0131764. doi: 10.1371 / journal.pone.0131764
- ↑ Стивън Д. Шеридан, Васуда Сурампуди, Радж Р. Рао, (2012). Анализ на ембриоидни тела, получени от индуцирани от човека плурипотентни стволови клетки като средство за оценка на плурипотентността, Stem Cells International, 2012, ID номер 738910,
- ↑ Тони-Мари Ачили, Джулия Майер, Джефри Р Морган, (2012). Напредък във формирането, използването и разбирането на многоклетъчни сфероиди, Становище на експертите по биологична терапия, 12 (10), 1347-1360 DOI: 10.1517 / 14712598.2012.707181
- ↑ Carpenedo RL, Sargent CY, McDevitt TC (2007) Ротационна суспензионна култура повишава ефективността, добива и хомогенността на диференциацията на ембрионалното тяло. Стволови клетки 25: 2224-2234. DOI: 10.1634 / стволови клетки.2006-0523
- ↑ Шкуматов А, Баек К, Конг Н (2014) Формиране на сърдечно-съдови органоиди, модулирани с твърдост на матрицата от ембриоидни тела. PLoS ONE 9 (4): e94764. Doi: 10.1371 / journal.pone.0094764
- ↑ Heras-Bautista, C. O., Katsen-Globa, A., Schloerer, N. E., Dieluweit, S., El Aziz, O. M. A., Peinkofer, G., ... & Pfannkuche, K. (2014). Влиянието на условията на физиологичната матрица върху трайната култура на индуцирани кардиомиоцити, получени от плурипотентни стволови клетки. Биоматериали, 35 (26), 7374-7385.
- ↑ Qiu, Y., Bayomy, A. F., Gomez, M. V., Bauer, M., Du, P., Yang, Y., ... & Liao, R. (2015). Роля на сковаността на матрицата в регулирането на сърдечната страна на популационната клетъчна функция. Американски вестник по физиология-сърдечна и циркулаторна физиология, 308 (9), H990-H997. DOI: 10.1152 / ajpheart.00935.2014
- ↑ Patel, A. K., Celiz, A. D., Rajamohan, D., Anderson, D. G., Langer, R., Davies, M. C., ... & Denning, C. (2015). Определен синтетичен субстрат за безсерумна култура на кардиомиоцити, получени от човешки стволови клетки, с подобрена функционална зрялост, идентифицирана с помощта на комбинации от микрочипове от комбинирани материали. Биоматериали. 61, 257-265. DOI: 10.1016 / j.biomaterials.2015.05.019
- ↑ Малкото биещо сърце, израснало от СТЪЛБОВИ КЛЕТКИ, Поща онлайн... Посетен на 2 юли 2017 г.
- ↑ Въпроси на сърцето: Изследователите създават 3-D биещо сърце (англ.), ScienceDaily... Посетен на 2 юли 2017 г.
- ↑ Анатолий Глянцев (2018). За първи път зряла сърдечна тъкан е отгледана от стволови клетки. "Vesti.Nauka" ()
- ↑ Ronaldson-Bouchard, K., Ma, S. P., Yeager, K., Chen, T., Song, L., Sirabella, D., ... & Vunjak-Novakovic, G. (2018). Усъвършенствано съзряване на човешка сърдечна тъкан, отгледана от плюрипотентни стволови клетки. Nature, 556, 239-243 DOI: 10.1038 / s41586-018-0016-3
- ↑ Таканори Такебе, Кейсуке Секине, Масахиро Еномура и др. & Hideki Taniguchi (2013) Васкуларизиран и функционален човешки черен дроб от трансплантация на органични пъпки, получена от iPSC. Nature DOI: 10.1038 / nature12271
- ↑ Човешки черен дроб, отгледан при мишки
- ↑ Хуч, М; Гехарт, Н; Van Boxtel, R; Хамер, К; Blokzijl, F; Верстеген, М. М.; Елис, Е; Ван Венум, М; Fuchs, S.A.; De Ligt, J; Ван Де Ветеринг, М; Сасаки, N; Boers, S. J.; Кемперман, Н; De Jonge, J; Ijzermans, J. N.; Nieuwenhuis, E.E.; Hoekstra, R; Стром, С; Vries, R. R.; Ван Дер Лаан, Л. Дж.; Cuppen, E; Clevers, H (2015). Дългосрочна култура на геномно-стабилни бипотентни стволови клетки от възрастен човешки черен дроб. Клетка 160 (1-2): 299-312. DOI: 10.1016 / j.cell.2014.11.050. PMC 4313365. PMID 25533785.
- ↑ Изследователите тестват биоискусствено чернодробно устройство за лечение на остра чернодробна недостатъчност (англ.), ScienceDaily... Посетен на 2 юли 2017 г.
- ↑ Takebe T. et al., & Taniguchi H. (2017). Масово и възпроизводимо производство на чернодробни пъпки изцяло от човешки плюрипотентни стволови клетки. Клетъчни доклади, 21 (10), 2661-2670. DOI: 10.1016 / j.celrep.2017.11.005
- ↑ Ogawa, M., Oshima, M., Imamura, A., et al. & Tsuji, T. (2013) Функционална регенерация на слюнчените жлези чрез трансплантация на биоинженерно зародишен орган. Nature Communications; 4, номер на артикул: 2498 DOI: 10.1038 / ncomms3498
- ↑ Hirayama, M., Ogawa, M., Oshima, M., et al. & Tsuji, T. (2013) Функционална регенерация на слъзната жлеза чрез трансплантация на биоинженерно зародишен орган. Nature Communications, 4, номер на артикул: 2497 DOI: 10.1038 / ncomms3497
- ↑ Литъл, М. Х. и Такасато, М. (2015). Генериране на самоорганизиращ се бъбрек от плурипотентни клетки. Актуално мнение в областта на трансплантацията на органи, 20 (2), 178-186. DOI: 10.1097 / MOT.0000000000000174
- ↑ Minoru Takasato, Pei X. Er, Han S. Chiu, et al., & Melissa H. Little (2015). Бъбречните органоиди от човешки iPS клетки съдържат множество линии и моделират човешката нефрогенеза. Природа, DOI: 10.1038 / природа15695
- ↑ Yokote, S., Matsunari, H., Iwai, S., Yamanaka, S., Uchikura, A., Fujimoto, E., ... & Yokoo, T. (2015). Стратегия за отделяне на урина за ембрионални бъбреци, генерирани от стволови клетки. Известия на Националната академия на науките, 201507803. DOI: 10.1073 / стр.1507803112
- ↑ Greggio, C., De Franceschi, F., Figueiredo-Larsen, M., Gobaa, S., Ranga, A., Semb, H., ... & Grapin-Botton, A. (2013) Изкуствен триизмерен ниши деконструират развитието на панкреаса in vitro. Развитие, 140 (21), 4452-4462. doi: 10.1242 / dev.096628
- ↑ Fan, Y., Tajima, A., Goh, S. K., Geng, X., Gualtierotti, G., Grupillo, M., ... & Trucco, M. (2015). Биоинженерни тимусни органоиди за възстановяване на тимусната функция и индуциране на специфична за донорите имунна толерантност към алотрансплантатите. Молекулярна терапия. DOI: 10.1038 / mt.2015.77
- ↑ Изкуственият тимус може да произвежда Т-клетки за борба с рака от кръвни стволови клетки. Посетен на 2 юли 2017 г.
- ↑ Christopher S Seet, et al., & Amélie Montel-Hagen (2017). Генериране на зрели Т клетки от човешки хематопоетични стволови и предшествени клетки в изкуствени тимусни органоиди. Nature Methods DOI: 10.1038 / nmeth.4237
- ↑ Dye, B. R., Hill, D. R., Ferguson, M. A., Tsai, Y. H., Nagy, M. S., Dyal, R., ... & Spence, J. R. (2015). In vitro генериране на белодробни органоиди, получени от човешки плурипотентни стволови клетки. Elife, 4, e05098. DOI:
- ↑ Дан С. Уилкинсън, Джаклин А. Алва-Орнелас, Дженифър М.С. Sucre et al., & Brigitte N. Gomperts (2016). Разработване на триизмерна биоинженерна технология за генериране на белодробна тъкан за персонализирано моделиране на заболявания. Стволови клетки Trans Med. DOI: 10.5966 / sctm.2016-0192
- ↑ Eiraku, M., Takata, N., Ishibashi, H., Kawada, M., Sakakura, E., Okuda, S., ... & Sasai, Y. (2011). Самоорганизираща се морфогенеза на оптична чаша в триизмерна култура. Природа, 472 (7341), 51-56.
- ↑ 3-D „мини-ретини“, отглеждани от миши и човешки стволови клетки (инж.), ScienceDaily... Посетен на 2 юли 2017 г.
- ↑ Manuela Völkner et al. & Mike O. Karl (2016). Органоидите на ретината от плурипотентни стволови клетки ефективно рекапитулират ретиногенезата. Доклади за стволови клетки DOI:
- ↑ Longworth-Mills, E., Koehler, K. R., & Hashino, E. (2015). Генериране на органоиди на вътрешното ухо от ембрионални стволови клетки на мишка. Методи в молекулярната биология, 10, 7651 DOI: 10.1007 / 7651_2015_215
- ↑ Calderon-Gierszal EL, Prins GS (2015) Насочена диференциация на човешки ембрионални стволови клетки в простатни органоиди In vitro и нейното смущение чрез експозиция на ниски дози бисфенол А. PLoS ONE 10 (7): e0133238. Doi: 10.1371 / journal.pone.0133238
- ↑ Lancaster, M. A., Renner, M., Martin, C. A., Wenzel, D., Bicknell, L. S., Hurles, M. E., ... & Knoblich, J. A. (2013). Церебралните органоиди моделират развитието на човешкия мозък и микроцефалията. Природа, 501 (7467), 373-379.
- ↑ Smith, I., Silveirinha, V., Stein, J. L., Torre-Ubieta, L., Farrimond, J. A., Williamson, E. M., & Whalley, B. J. (2015). Културите на човешки невронни стволови клетки в триизмерни субстрати образуват спонтанно функционални невронни мрежи. Вестник за тъканно инженерство и регенеративна медицина. DOI: 10.1002 / срок.2001.
- ↑ Harris, J., Tomassy, G. S. and Arlotta, P. (2015), Строителни блокове на мозъчната кора: от развитието до ястието. WIREs Dev Biol. doi: 10.1002 / wdev.192
- ↑ Anca M Paşca, Steven A Sloan, Laura E Clarke, Yuan Tian, Christopher D Makinson, Nina Huber, Chul Hoon Kim, Jin-Young Park, Nancy A O'Rourke, Khoa D Nguyen, Stephen J Smith, John R Huguenard , Daniel H Geschwind, Ben A Barres, Sergiu P Paşca (2015). Функционални кортикални неврони и астроцити от човешки плурипотентни стволови клетки в 3D култура. Природни методи; DOI: 10.1038 / nmeth.3415
- ↑ Рене Ананд (2015) Учени отглеждат човешки фетален мозък в лабораторна чиния от стволови клетки. Scicasts
- ↑ Юрген Кноблич Как да изградим мозък // В света на науката. - 2017. - No 3. - С. 40 - 44.
- ↑ Stuart M. Chambers, Jason Tchieu, Lorenz Studer Изграждане на мозък // Клетъчна стволова клетка. -2013-10-03. - Т. 13, не. 4. - С. 377–378. - DOI: 10.1016 / j.stem.2013.09.010.
- ↑ Schwartza, M P., Houb, Z, Propson N E. et al. & Thomson JA (2015). Невронни конструкции, получени от човешки плурипотентни стволови клетки, за предсказване на невронна токсичност. Сборник на Националната академия на науките, DOI: 10.1073 / pnas.1516645112
- ↑ Никълъс С. Зачос, Олга Ковбанюк, Дженифър Фулке-Абел, Джули Ин, Сара Е. Блут Човешки ентероиди / колоноиди и чревни органоиди функционално рекапитулират нормалната чревна физиология и патофизиология // Вестник по биологична химия. -19.02.2016 г. - кн. 291, бр. 8. - С. 3759-3766. -ISSN 1083-351X 0021-9258, 1083-351X. - DOI: 10.1074 / jbc.r114.635995.
- ↑ Дюжева Т.Г., Люндъп А.В., Клабуков И.Д., Чвалун С.Н., Григориев Т.Е., Шепелев А.Д., Тенчурин Т.Х., Крашенинников М.Е., Оганесян Р.ИН. Перспективи за създаване на тъканно-конструиран жлъчен канал // Гени и клетки. - 2016. - Т. 11, No 1. - С. 43-47. - ISSN 2313-1829.
- ↑ Mahe, M. M., Sundaram, N., Watson, C. L., Shroyer, N. F., & Helmrath, M. A. (2015). Създаване на човешки епителни ентероиди и колоноиди от цяла тъкан и биопсия. Списание за визуализирани експерименти: JoVE, (97). 52483. DOI: 10.3791 / 52483
- ↑ Lukovac, S., & Roeselers, G.(2015). Органоиди на чревната крипта като експериментални модели. В The Impact of Food Bioactives on Health (стр. 245-253). Международно издателство Springer. DOI: 10.1007 / 978-3-319-16104-4_22
- ↑ van de Wetering, M., Francies, H. E., Francis, J. M., Bounova, G., Iorio, F., Pronk, A., ... & Clevers, H. (2015). Проспективно извличане на жива органоидна биобанка на пациенти с колоректален рак. Клетка, 161 (4), 933-945. DOI:
- ↑ Higgins C. A., Chen J. C., Cerise J. E., et al. & Christiano A. M. (2013) Препрограмирането на микросредата чрез триизмерна култура позволява на дермалните папилални клетки да индуцират растежа на човешки космен фоликул de novo. PNAS, doi: 10.1073 / pnas.1309970110
- ↑ Биоботове, задвижвани от мускули, ходят по команда (eng.), ScienceDaily... Посетен на 2 юли 2017 г.
- ↑ Madden, L., Juhas, M., Kraus, W. E., Truskey, G. A., & Bursac, N. (2015). Биоинженерните човешки миоснопчета имитират клиничните реакции на скелетните мускули към лекарства. eLife. DOI:
- ↑ Моримото, Ю., Като-Негиши, М., Оное, Х. и Такеучи, С. (2013). Триизмерни невронно-мускулни конструкции с невромускулни връзки. Биоматериали, 34 (37), 9413-9419.
- ↑ Марк Джухас, Джордж С. Енгелмайр -младши, Андрю Н. Фонтанела, Грегъри М. Палмър и Ненад Бурсак (март 2014 г.). Биомиметично проектиран мускул с капацитет за съдова интеграция и функционално съзряване in vivo. PNAS, DOI: 10.1073 / pnas.1402723111
- ↑ Кирил Стасевич (април 2014 г.). ИЗКУСТВЕНИТЕ МИСКУЛИ СА НАЛИЧНИ ЗА САМОЛЕЧЕНИЕ. КОМПУЛЕНТНО
- ↑ Клаудия Фуоко, Роберто Рици, Антонела Биондо и др., (2015). n vivo генериране на зрял и функционален изкуствен скелетен мускул. EMBO Molecular Medicine, DOI: 10.15252 / emmm.201404062
- ↑ Инженерите отглеждат функциониращи човешки мускули от кожни клетки
- ↑ Иларио Фулко, Силви Миот, Мартин Д Хауг и др. (2014). Конструирана автоложна хрущялна тъкан за реконструкция на носа след туморна резекция: наблюдение първо при хора. Ланцетът. DOI: 10.1016 / S0140-6736 (14) 60544-4
- ↑ Atlántida M Raya-Rivera, Diego Esquiliano, Reyna Fierro-Pastrana и др. & Антъни Атала. (2014). Инструментирани от тъкани автоложни вагинални органи при пациенти: пилотно кохортно проучване. Ланцетът; DOI: 10.1016 / S0140-6736 (14) 60542-0
- ↑ Стасевич К. ВАГИНА ОТ ТЕСТОВА ТЪРБА Е УЧАСТВАНА В ЧОВЕШКИЯ ОРГАНИЗЪМ. КОМПУЛЕНТНО
- ↑ Jyothsna Vasudevan, Jyothsna Vasudevan. Човешки хранопровод, създаден от 3D скеле, изпълнено със стволови клетки. Biotechin.Asia.25 август 2015 г. Посетен на 2 юли 2017 г.
- ↑ Zhili Rong, Meiyan Wang, Zheng Hu, et al. &, Xuemei Fu. (2014) Ефективен подход за предотвратяване на имунно отхвърляне на човешки алотрансплантати, получени от ESC. Клетъчна стволова клетка; 14 (1): 121 DOI: 10.1016 / j.stem.2013.11.014
- ↑ Plege-Fleck A, Lieke T, Römermann D, Düvel H, Hundrieser J, Buermann A, Kraus L, Klempnauer J, Schwinzer R. Трансплантация на прасе към плъх: редуцирани и антитела реакции към свръхекспресиращи PD-L1 ксенотрансплантати. Ксенотрансплантация 2014; 21: 533-542. DOI: 10.1111 / xen.12121
- ↑ Щитовидната жлеза, създадена с помощта на 3D биопечат, беше успешно трансплантирана в мишки (руски). Посетен на 2 юли 2017 г.
- ↑ Елена А. Буланова, Елизавета В. Кудан, Джонатан Дегосери, Шарлот Хейманс, Фредерико ДАС Перейра Биопечатване на функционална васкуларизирана мишка щитовидна жлеза (английски) // Биофабрикация. - 2017. - Т. 9, бр. 3. - С. 034105. - ISSN 1758-5090. - DOI: 10.1088 / 1758-5090 / aa7fdd.
- ↑ Мозайка, Moheb Costandi -... Човекът, който израства очи от нулата (eng.), Gizmodo... Посетен на 2 юли 2017 г.
- ↑ Bement, W. M., & von Dassow, G. (2014). Образуване на единични клетъчни модели и преходни цитоскелетни масиви. Актуално мнение в клетъчната биология, 26, 51-59.
- ↑ Ishihara, K., Nguyen, P. A., Wühr, M., Groen, A. C., Field, C. M., & Mitchison, T. J. (2014). Организация на ранните ембриони на жаби чрез химически вълни, излъчвани от центрозоми. Философски сделки на Кралското общество В: Биологични науки, 369 (1650), 20130454.
- ↑ Karus, M., Blaess, S., & Brüstle, O. (2014). Самоорганизация на архитектурите на нервната тъкан от плюрипотентни стволови клетки. Списание за сравнителна неврология.
- ↑ S.A. Живолупов, Н.А. Рашидов, И.Н. Самарцев, Е.В. Яковлев Съвременни представи за регенерацията на нервните влакна при наранявания на периферната нервна система // Известия на Руската военномедицинска академия. - 2013. - No 3 (43). - С. 190-198. - ISSN 1682-7392.
- ↑ Greggio, C., De Franceschi, F. и Grapin-Botton, A. (2015), кратки рецензии: In Vitro произведени модели на органогенеза на панкреаса в три измерения: самоорганизация от няколко стволови клетки или предшественици. СТВОЛНИ КЛЕТКИ, 33: 8-14. DOI: 10.1002 / стъбло 1828
- ↑ Барановски Д. С., Демченко А. Г., Оганесян Р. В., Лебедев Г. В., Берсенева Д. А., Балясин М. В., Паршин В. Д., Люндюп А. В. Получаване на безклетъчна матрица от хрущял на трахеята за конструкции на тъканно инженерство (руски) // Бюлетин на Руската академия на медицинските науки. - 2017.- Т. 72, бр. 4. - С. 254–260. - ISSN 2414-3545. - DOI: 10.15690 / vramn723.
- ↑ Люндъп А.В., Демченко А.Г., Тенчурин Т.Х., Крашенинников М.Е., Клабуков И.Д., Шепелев А.Д., Мамагулашвили В.Г., Оганесян Р.В., Орехов А.Н., Чвалун С.Н., Дюжева Т.Г. Повишаване на ефективността на колонизация на биоразградими матрици със стромални и епителни клетки по време на динамично култивиране // Гени и клетки. - 2016. - Т. 11, No 3. - С. 102-107. - ISSN 2313-1829.
- ↑ Екипът на MGH разработва трансплантируеми биоинженерни предни крайници в животински модел. Обща болница в Масачузетс. Посетен на 2 юли 2017 г.
- ↑ На крайник: Учени -пионери отглеждат маймунски ръце в лабораторията. WGNO.11 август 2015 г. Посетен на 2 юли 2017 г.
- ↑ Bernhard J. Jank, Linjie Xiong, Philipp T. Moser et al. & Harald C. Ott (2015). Конструирана композитна тъкан като био изкуствена присадка на крайник. Биоматериали, 61, 246-256 DOI: 10.1016 / j.biomaterials.2015.04.051
- ↑ Функционален сърдечен мускул, регенериран в децелуларизираните човешки сърца. Посетен на 2 юли 2017 г.
- ↑ Guyette JP, Charest JM, Mills RW, Jank BJ, Moser PT, Gilpin SE, Gershlak JR, Okamoto T, Gonzalez G, Milan DJ, Gaudette GR, Ott HC. (2015). Биоинженеринг на човешки миокард върху естествен извънклетъчен матрикс. Circ Res.; 118 (1), 56-72. DOI: 10.1161 / CIRCRESAHA.115.306874 PMID 26503464
- ↑ Петербургски лекари са инсталирали биоинженерна протеза на трахеята (руски). Посетен на 2 юли 2017 г.
Литература
- Руски учени създадоха био-изкуствен черен дроб. 3 септември 2014 г., 14:39
- Андрей Константинов (2014). Сърце от биореактора "Руски репортер" № 19 (347)
- Виктория Севостьянова (2014) Нуждаете се от нова аорта? Отглеждайте го сами !. НАУКА И ЖИВОТ, 04
- Кирил Стасевич (2015). Как да отглеждаме мозък в епруветка. НАУКА И ЖИВОТ No6
- Кирил Стасевич (2014). Човешкият стомах е отгледан в епруветка. НАУКА И ЖИВОТ № 10
- Кондратенко Юлия (2015). Органи от лабораторията.
- Рупърт Уингфийлд -Хейс (2014) Япония иска да отглежда органи при прасета за хората от Би Би Си, префектура Ибараки, Япония - Видео.
- Akkerman, N., & Defize, L. H. (2017). Зората на ерата на органоидите. БиоЕсета. DOI: 10.1002 / bies.201600244 Прегледна статия за предварително запознаване с методите за отглеждане на органели и техните проблеми
- Takebe, T., Enomura, M., Yoshizawa, E., Kimura, M., Koike, H., Ueno, Y., ... & Taniguchi, H. (2015). Васкуларизирани и сложни органни пъпки от различни тъкани чрез мезенхимална клетъчна кондензация. Клетъчна стволова клетка, 16 (5), 556-565. DOI:
- Yin, X., Mead, B. E., Safaee, H., Langer, R., Karp, J. M., & Levy, O. (2016). Инженерни органоиди на стволови клетки. Клетъчна стволова клетка, 18 (1), 25-38. DOI:
- Yunying Liu, Ru Yang, Zuping He и Wei-Qiang Gao (2013) Генериране на функционални органи от стволови клетки. Регенерация на клетки, 2: 1 doi: 10.1186 / 2045-9769-2-1
- Кели Рей Чи (2015). Организиране на органоиди. Ръководство за изработване на тъкани в чиния, които пресъздават in vivo органи. Ученият.
- Наръчник за отглеждане. и използването на органели (2016 г.). Наръчник за органоидна култура
- Кан Ханда, Кентаро Мацубара, Кен Фукумицу, Хорхе Гусман-Лепе, Алисия Уотсън, Алехандро Сото-Гутиерес. Събиране на човешки органи от стволови клетки за изследване на чернодробно заболяване // The American Journal of Pathology. - 2014. - Т. 184, не. 2. - С. 348-357. -DOI: 10.1016 / 0092-8674 (83) 90040-5.
- Мелиса А. Кини, Трейси А. Хукуей, Юн Уанг, Тод С. Макдевит (декември 2013 г.) Инженерна триизмерна морфогенеза на стволови клетки за разработване на тъканни модели и мащабируема регенеративна терапия. Анали на биомедицинското инженерство. DOI: 10.1007 / s10439-013-0953-9
- Очи в лаборатория - Видео "Как са отгледани очите на жив заек."
- Хитоми Мацунари, Хироши Нагашима, Масахито Ватанабе и др. и Хиромицу Накаучи (2013). Комплементацията на бластоцисти генерира екзогенен панкреас in vivo при клонирани прасета в панкреаса. PNAS, 110 (12), 4557-4562, doi: 10.1073 / pnas.1222902110
- Feng, W., Dai, Y., Mou, L., Cooper, D. K., Shi, D., & Cai, Z. (2015). Потенциалът на комбинацията от CRISPR / Cas9 и плюрипотентни стволови клетки за осигуряване на човешки органи от химерски прасета. Международно списание за молекулярни науки, 16 (3), 6545-6556. DOI: 10.3390 / ijms16036545
- Като живо, биещо сърце се отглежда от стволови клетки. ЗАДЪЛЖИТЕЛНО ГЛЕДАЙТЕ ВИДЕО
- Christa Nicole Grant, Garcia Mojica Salvador, Frederic G Sala et al. (2015). Тънките черва, проектирани от човек и мишка, демонстрират храносмилателна и абсорбираща функция. Американски вестник по физиология- Стомашно-чревна и чернодробна физиология, DOI: 10.1152 / ajpgi.00111.2014
- Donghui Zhang и Wei Jiang (2015). От едноклетъчни до тъкани: препрограмиране, клетъчно диференциране и тъканно инженерство. BioScience, doi: 10.1093 / biosci / biv016
- Касандра Уилярд (2015). Бумът на мини стомаси, мозъци, гърди, бъбреци и др. Nature 523, 520-522 DOI: 10.1038 / 523520a
- Изтеглете ръководство за приложение: Органоид (органоподобни структури, които могат да се образуват чрез 3D клетъчна култура) Растеж на BME 2.
- Purwada, A., Jaiswal, M. K., Ahn, H., Nojima, T., Kitamura, D., Gaharwar, A. K., ... & Singh, A. (2015). Ex vivo създадени имунни органоиди за контролирани реакции на зародишен център.Биоматериали, 63, 24-34. DOI: 10.1016 / j.biomaterials.2015.06.002
- Broutier, L., Andersson-Rolf, A., Hindley, C. J., Boj, S. F., Clevers, H., Koo, B. K., & Huch, M. (2016). Култура и установяване на самообновяващи се 3D органоиди от черен дроб и панкреас на възрастни хора и мишки и тяхната генетична манипулация. Природни протоколи, 11 (9), 1724-1743. DOI: 10.1038 / nprot.2016.097
- García-Domínguez, X., Vera-Donoso, C. D., García-Valero, L., Vicente, J. S., & Marco-Jimenez, F. (2016). Ембрионална трансплантация на органи: новата ера на ксенотрансплантацията. В границите на трансплантологията. InTech. DOI: 10.5772 / 62400
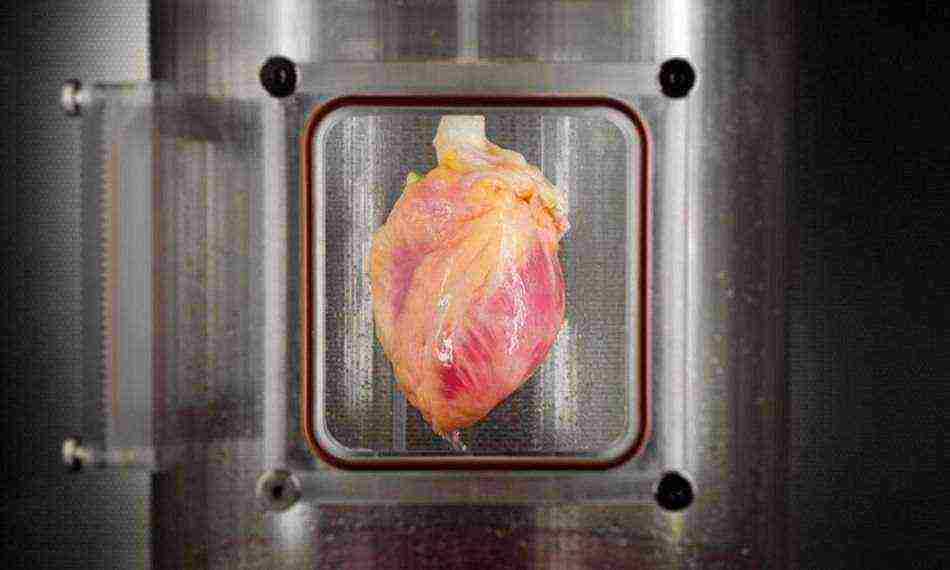
Хиляди хора по света чакат донорски сърца, които могат да спасят живота им. Но само няколко от тях получават такъв шанс и като се има предвид, че тялото може да отхвърли чужд орган, това значително намалява броя на успешните трансплантации. Учените отдавна работят за решаването на този проблем и сега екип от изследователи от Централната болница в Масачузетс, заедно със служители на Харвардското медицинско училище, са много близо до създаването на изкуствено отгледани сърца.
Американски учени са отгледали човешка сърдечна тъкан в лабораторни условия, както се съобщава в списанието. За тяхното създаване са използвани кожни клетки на възрастен. В идеалния случай всичко това в бъдеще трябва да доведе до култивиране на пълноценни биещи сърца от клетките на онези хора, които се нуждаят от трансплантация на орган. Органите се отглеждат много по -лесно в лаборатория, където учените имат някакви скелета за бъдещи органи, чрез които се разпределят клетките.
В предишната си работа учените са създали технология, която ви позволява да изключите имунния отговор на тялото на реципиента при трансплантация на орган от друго лице. Те успяха да постигнат това, като премахнаха определени клетки, потенциално способни да предизвикат имунен отговор, от донорския орган, използвайки разтвор на детергент. Учените пренаселиха останалата извънклетъчна матрица със съответния тип клетки, съвместими с реципиента. По този начин учените вече са успели да създадат напълно функциониращи бъбреци и бели дробове за лабораторни плъхове.
Следващата стъпка на учените беше да експериментират с истинско човешко сърце в специално създаден биореактор. Органът беше изчистен от потенциално опасни клетки, след което останалото скеле беше повторно заселено със сърдечни клетки. Експериментите са проведени върху 73 човешки сърца, които са предоставени на изследователите от една от банките на органи. Не се притеснявайте, тези сърца все още бяха обявени за негодни за трансплантация, така че не можеха да спасят ничий живот.
За да получат сърдечни клетки, изследователите са използвали нов метод. Те препрограмират кожни клетки за възрастни, използвайки посланни РНК фактори, което причинява по -малко затруднения при последващото регулиране на процесите. Получените плурипотентни стволови клетки се диференцират в сърдечни мускулни клетки. Получените клетки бяха напълно достатъчни за изследване и тяхната трансплантация върху сърдечни скелета. Вече няколко дни по -късно учените успяха да растат спонтанно свиващи се мускулни тъкани върху скелета.
За първи път учените успяха да регенерират човешкия сърдечен мускул от плурипотентни стволови клетки в безклетъчната матрица на цялото човешко сърце. Те са трансплантирали около 500 милиона клетки в стената на лявата камера на орган, лишен преди това от сърдечни клетки. След това сърцето остана в автоматизираната система за биореактори две седмици. През това време учените снабдяват сърцето с хранителен разтвор и действат върху него с различни фактори на стреса. В резултат на това клетките се трансформират в незряла сърдечна тъкан, която реагира на електрическа стимулация.
Разбира се, досега всичко това са само експерименти, но, трябва да се отбележи, техните резултати са много обещаващи. В бъдеще подобна технология може да се развие в пълноценно култивиране на човешки сърца ин витро, което ще може да даде втори шанс на онези хора, които от години чакат подходящ донорски орган.


